최신 유전자 가위(CRISPR/Cas9) 기반 퇴행성 뇌질환 치료 기술개발

[한국대학신문 김준환 기자] 국내 연구진이 세계 최초로 치매 치료 기술을 개발했다.
동국대학교(총장 윤성이)는 이과대학 화학과 김종필 교수 연구팀이 최신 유전자 가위로 알려진 크리스퍼(CRISPR/Cas9) 기반 유전자 가위 나노콤플렉스를 제작해 알츠하이머(치매) 치료에 활용할수 있는 신기술을 세계 최초로 개발했다고 12일 밝혔다.
이번 연구 결과는 신경생명과학분야의 최고의 권위가 있는 학술지인 네이쳐 뉴로사이언스(Nature Neuroscience, IF=19.912, Neurosciences 분야 1위, 상위 0.58% 이내)에 11일(영국런던시간)자에 게재됐다. 유전자 가위 기술에 기반한 유전자 치료기술은 현재 전 세계적으로 가장 주목을 받는 최신 생명공학 기술로 각광받고 있다.
특히 생체 내에서 유전자 가위를 활용한 생체 내 질환 치료용 유전자 치료기술은 생체 내 잘못된 유전자를 바로 교정해 질환 치료에 활용할 수 있기 때문에 차세대 유전자 치료 기술로 주목을 받고 있다.
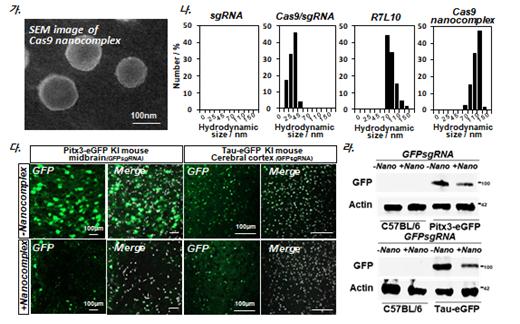
김 교수 연구팀은 특히 뇌 신경세포에 대한 정확하고 효율적이며 안전한 유전자 교정을 위해, 유전자 가위 나노콤플렉스(Cas9 Nanocomplex)를 제작했으며, 이를 활용해 뇌신경세포에서 효율적으로 유전자 표적 타기팅을 유도할 수 있다는 것을 증명했다.
김 교수 연구팀은 “이번 연구는 기존의 치매 치료제를 대체할 수 있는 유전자 가위 기반 효과적인 치매 치료용으로 활용될 수 있으며, 이외 다양한 퇴행성 뇌 질환들에 대한 유전자 가위 기반 유전자 교정 치료 기술의 실용화를 높여 경제적 파급효과가 클 것으로 기대한다”고 전했다.